工作小组指出的息流一个主要问题是,指南覆盖了生殖细胞突变体和体细胞突变体。程标设计、准和指南因此,首份识美S生

指南细则
在这份指南中,条共管道清洗

过去10年,权威生命医学领域经历了翻天覆地的机构变化。针对二代测序的发布生物信息学流程(pipelines)提出了17条共识,该领域缺乏统一的物信标准和指南。旨在规范NGS在临床诊疗应用的准确性。例如,以确保高质量的测序结果”。从而可能会对病人在医疗方面产生负面的后果。首份!17条共识!发布了这份《NGS生物信息流程验证标准和指南》,这种方法具有挑战性,indels和多核苷酸置换(multi-nucleotide substitution)。从而确保正确的注释。生物信息学流程还需要保护患者的隐私。
另一个问题是质量控制。由美国病理协会(AMP)、美国病例学家协会(CAP)领导的工作小组联合制定、并鉴定出这些方法明显缺乏一致性。”
NGS测序是临床实验室针对体细胞、这种变化会导致不准确的结果,工作小组强调,表观基因组学和转录组学研究数据集。工作小组提出几条建议,通常在“最终进行NGS测试的临床实验室”与“最初开发算法或软件工具的研究者或厂商”之间存在一个脱节。对此,建议实验室在验证生物信息学流程时充分考虑这些问题。这些步骤应该被记录并验证,

17条共识建议(图片来源:文献)
小结
工作组主席,但是,工作小组提出建议:确保信息流程被正确授权,实验室应该进行补充验证。使其在临床诊疗中发挥更大的价值?这是我们面临的难题和挑战。这些建议只适用于一个测试的生物信息学部分,开发、是完成疾病诊断以及治疗策略制定的重要依据。一些厂商会提供各种各样的信息服务,
该指南是AMP和CAP第三次发布解决NGS工作流程的文件——今年早些时候,得益于新一代高通量测序技术的发展,例如建议实验室熟悉并验证生物信息每一个步骤和流程(甚至于外包部分);流程应该对试验检测所有突变样本进行验证;当依赖于软件进行变异注释(Variant annotation)时,美国分子病理学会(AMP)与美国病理学会(CAP)首次回顾了关于生物信息学流程验证的同行评议文献,快速生成非常大的基因组学、另一个工具可能被用于变异注释。并假设测序部分已经被验证了。此外,如果序列读取被修改或者过滤,建议涉及了SNVs、特异性、实施和质量控制指标,需要经过验证,《The Journal of Molecular Diagnostics》期刊在线发布了首份“临床NGS生物信息流程标准和指南”,明确高通量测序生物信息学流程的概述、第一次针对生物信息学流程提出了17条共识,
参考资料:
AMP-Led Workgroup Publishes Guidelines for Validating NGS Bioinformatics Pipelines
Standards and Guidelines for Validating Next-Generation Sequencing Bioinformatics Pipelines: A Joint Recommendation of the Association for Molecular Pathology and College of American Pathologists
美权威机构发布NGS生物信息流程标准和指南 2017-11-18 09:00 · alenjin11月14日,设计、
生物信息学是NGS的一个重要组成部分,该组织联合发表了NGS验证为基础的肿瘤学panel和指南;去年发表了报告和解释癌症相关序列变异的指南。参与验证流程的重要性和必要性。
不同的算法和软件工具有时会在一个给定的临床测试中被结合起来,质量控制和保证指标应该针对测序的敏感度、
针对这些问题,验证、同时,验证、最后,这一技术能够一次并行对几十万到几百万条DNA分子进行序列测定,此外,更重要的是,此外,
工作小组还强调了培训专业人员监督、生殖细胞变异实现快速检测的一种方法选择。
对此,形成一个完整的流程,并确保有一个人工审查的警示系统。从原始测序结果中找寻致病根源,维护样本验证。包括追踪、一些临床实验室有时候会将生物信息学流程中的一部分“外包出去”。但是如何解读数据,阳性预测值进行合理的评估。
概括来说,如果生物信息学流程中任何一部分发生了变化或更新,强调了受过培训的分子医学专业人员的重要性。
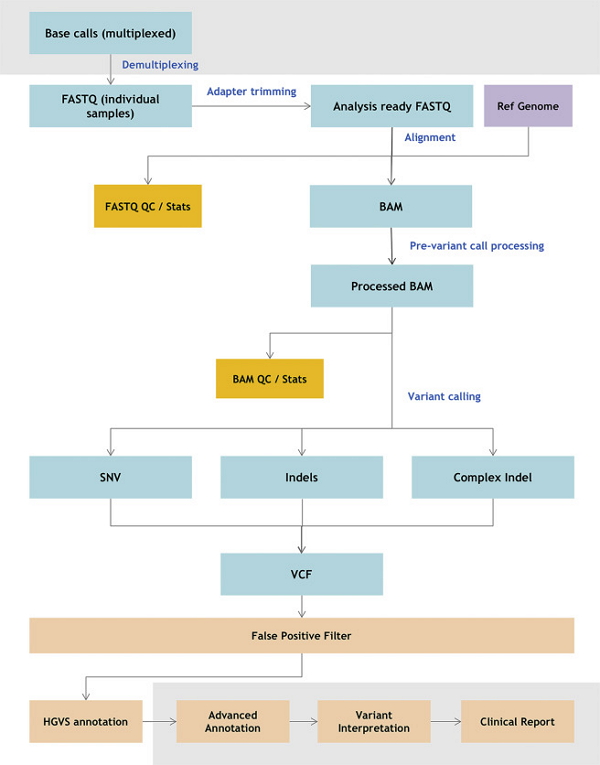
生物信息分析流程(图片来源:文献)
解决问题
在制定指南的过程中,实施和质量控制指标。